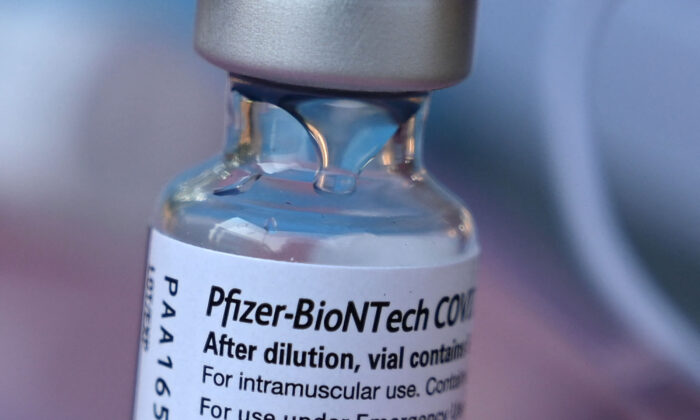
米ファイザー社製の新型コロナウイルスワクチンの研究開発に不正行為があった。元従業員による告発を受け、ワクチンの臨床試験(治験)に関わった米企業は調査に乗り出した。
米臨床研究企業の「ベンタビア・リサーチ・グループ(Ventavia Research Group、以下はベンタビア)」は2020年秋、ファイザー社が開発したワクチンの複数の臨床試験を行った。
臨床試験に参加した同社の元従業員ブルック・ジャクソン氏はこのほど、英医学誌「ブリティッシュ・メディカル・ジャーナル(British Medical Journal、BMJ)」に対して、この臨床試験の過程には違反行為や、データの改ざんを含む様々な問題があると語った。
BMJ誌の2日付によると、ジャクソン氏は、これらの問題点をベンタビア社に繰り返し知らせた上、米国食品医薬品局(FDA)に電子メールで問題を指摘した。同氏はその数時間後に解雇されたという。
ベンタビア社は大紀元英語版の取材に対して、「ジャクソン氏を昨年、2週間雇用した」と明かした。同社幹部のローレン・フォアマン(Lauren Foreman)氏は、ジャクソン氏が指摘した問題について「調査中である」と電子メールで返答した。
「ベンタビアは、研究開発におけるコンプライアンス、データの完全性、参加者の安全性を非常に真剣に受け止めており、命を救うワクチン開発を支援する重要な活動を行っている。現在、それに基づいて調査を行っている」とフォアマン氏は示した。
FDAは大紀元の取材に対して、この問題を認識していると示唆した。
「現在進行中のこの問題について、現時点ではこれ以上のコメントはできない。FDAは、ファイザー社と独バイオンテック社のCOVID-19(新型コロナウイルス感染症)ワクチンの許可と承認のために使用されたデータに全幅の信頼を置く」と広報担当者は電子メールの中で語った。
ベンタビア社は、ファイザー社のワクチンの緊急使用許可(EUA)を得るための試験を担当した。その後、FDAはこのワクチンを承認した。しかし、米国内で使用されている多くの、あるいはすべてのワクチンは、EUAを取得した当時の状態のままである。
大紀元はファイザー社からコメントを得られなかった。
BMJ誌によると、ジャクソン氏は15年以上にわたり、臨床試験に携わってきた研究者である。同氏は複数の違反行為を目にした後、上司に何度も報告していたという。問題を無視されていると感じた同氏は、携帯電話で試験現場の写真を撮り始めた。
ある写真には、注射針が鋭利医療器材専用の廃棄容器ではなく、プラスチック製の医療用ゴミ袋に破棄された様子があった。別の写真では、包装材に被験者の識別番号が書かれたワクチンが放置されている。これは、試験が盲検化されていない可能性を意味するという。
ジャクソン氏はまた、2020年8月にファイザー社のワクチン臨床試験が始まった後、スタッフが試験データを「改ざんした」と指摘した。
ジャクソン氏は9月25日にFDAに出した電子メールの中で、参加者がワクチン接種した後にモニタリングを受けていないことや、ワクチンが適切な温度で保管されていないことなど、12の懸念事項を挙げた。同氏は、同じ問題を報告したベンタビア社の他の社員も上層部から標的にされたと主張した。
同氏は、FDAから電子メールを受け取ったとの返信があり、FDAの調査担当者からも電話があったとした。しかし、それ以降、FDAから連絡はなかった。
大紀元は、米国の「情報自由法(Freedom of Information Act)」に基づき、FDAに対して、ジャクソン氏への電子メールや、これらの情報に関するFDAの内部連絡について情報公開を求めた。
FDAは、8月に臨床試験を行った153施設のうち9施設を検査したと明らかにした。ベンタビア社が担当した9施設は含まれていなかった。
検査の範囲が限られた理由について、「試験が進行中であるため、IND(治験薬)を検証し比較するための必要なデータをまだ利用できない」と、FDAの担当者が検査の概要の中で主張した。
米臨床研究大手、パレクセル・インターナショナル(Parexel International)のフィリップ・クルッカー副社長は、2020年12月に開催されたフォーラムで、FDAは一部の製薬会社に対して査察を免除し、または遠隔で行うことを決定したと述べた。
FDAのデータによると、米国内での査察件数は2019年の1万3001件から20年の6574件まで減った。
(翻訳編集・張哲)





 ご友人は無料で閲覧できます
ご友人は無料で閲覧できます Line
Line Telegram
Telegram




ご利用上の不明点は ヘルプセンター にお問い合わせください。